Hola a todos

Introducción
La enseñanza de las ciencias ha variado durante el pasar de los años. Antes era considerado por algunos, y aunque hoy todavía lo piensan, que la finalidad de este tipo de enseñanza es para formar a los científicos del futuro. Sin embargo, no todos están bajo esta concepción. Por otro lado, otro grupo considera que es parte fundamental de la vida para poder afrontar los restos de nuestra sociedad y por ende del mundo. Con ello, los profesores de ciencia deben cumplir con una labor relevante hacia los estudiantes durante sus experiencias escolares.
En este sentido, el docente busca una cantidad de estrategias y actividades para que los estudiantes analicen, interpreten, corroboren y contrasten los hechos científicos o las teorías que puedan encontrarse durante la explicación de cualquier clase de ciencia. De allí, que actividades empíricas como las prácticas de laboratorio, en el marco de la enseñanza de la ciencias, cobran más valor académico. El laboratorio, es un espacio donde los alumnos pueden experimentar determinadas teorías o hipótesis que se plantean durante las clases.

Con lo antes mencionado, y como en otras ocasiones los estudiantes realizaron la práctica conjuntamente con el docente. De igual manera, se determinó los criterios para el protocolo de laboratorio, siguiendo los pasos teóricos y práctica para que la experiencia sea significativa.
Breve explicación teórica
La llama es aplicada en la práctica de laboratorio como una fuente que generada energía, a través de combustión de determinado gas formando una muestra luminosa, el cual desprende calor. Esto nos indica, que la llama tiene una fuente luminosa, y una fuente térmica. A su vez, dependiendo como se regule la entrada de aire, por ejemplo en un mechero Bunsen, puede llegar a actuar como oxidante o reductora. Una combustión con mayor presencia de O2 genera una llama oxidante, mientras que con defecto de O2 genera una combustión reductora. En este sentido, vale decir que la totalidad de la llama, tiene regiones consideradas oxidantes y regiones consideradas reductoras.
Ahora bien, los ensayos de coloración en la llama, llamados también ensayos por vía seca, debido a que las muestras a examinar no se someten a ningún cambio o modificación previa, son reacciones donde no se emplean solventes o disolvente. Estos ensayos permiten en un tiempo corto y con mínimas cantidades de muestra, determinar un buen número de sus propiedades como por ejemplo volatilidad, descomposición térmica, poder de coloración a la llama, entre otros.

Es conocida por ser una práctica con método analítico, para ver el espectro de emisión, el cual es característico en cada uno de los elementos. Cuando las muestras son llevadas a la llama de un mechero sus electrones externos se excitan. Al regresar al nivel de energía original, los electrones emiten la energía ganada en forma de luz, cuyo color va a depender de la longitud de onda de la luz emitida.
Vale acotar, que la coloración en la llama es debido a que determinados electrones cambian de niveles de energía. Y, en una mezcla, los elementos expresan su coloración, es decir que cada uno de estos elementos muestra un color diferente al de otro. También, es importante decir que entre los elementos, la intensidad de algunos es mayor que la de otros.
Momento de la práctica de laboratorio
Materiales de la práctica
- Mechero
- Alambre metálico
- Muestra de sales
- Ácido clorhídrico
- 5 vidrios de reloj
- Crisol de pico
- Agua destilada
- Cuaderno de anotaciones
- Encendedor
- Demás accesorios, tales como pañuelo.

Desarrollo de la práctica
- Limpia el alambre metálico sumergiéndolo en ácido clorhídrico y luego en agua destilada.
- Sécalo con el mechero. Colocas la punto donde va a ir la muestra en la llama.
- Repite el paso 1 hasta que el alambre no de ninguna coloración a la llama.

- Con el alambre metálico limpio toma una pequeña cantidad de una de las muestras y llévalas a la llama del mechero.
- Sostén el alambre en la punto del cono entre la llama.
- Anota el color de la llama para la muestra que examinaste.
- NOTA: Humedece las muestras a examinar con ácido clorhídrico, ya que los cloruros muestran mayor volatilidad.
- Repite los pasos 1,2,3 y 4, para las otras muestras de prueba.
A continuación se muestra la tabla de datos de la práctica:
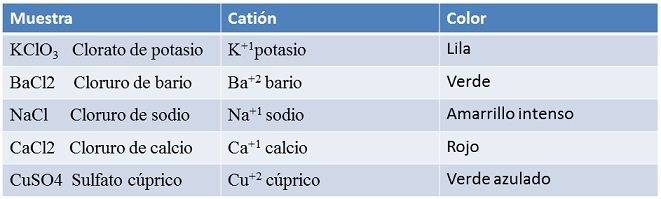
Nota final
En las prácticas de laboratorio los estudiantes lograron contrastan lo expresado durante las clases de manera teórica. Además, no esta de más señalar que generar curiosidad por los aspectos cientificos es de suma importancia para formar a ciudadanos con una formación sobre la ciencia. En la biología, conocer los aspectos sobre el espectro de luz es importante para conectar con contenidos como la diversidad en la naturaleza.
Fuente de las imágenes y del video
- Cada una de las imágenes son propias, editadas en power point y paint. De igual manera, el video es propio y subido a mi cuenta personal de youtube.
Referencia bibliográfica
- Martín. 2012. Enseñanza de las ciencias ¿Para qué?
- Quimitube. Colores que hablan: ensayos de coloración a la llama para los elementos químicos. Consultado: 2018.
- Ensayos a la llama. Material de apoyo de la UCV. Lab., movil y recursos. Consultado: 2018
Hi @hogarcosmico!
Your post was upvoted by utopian.io in cooperation with steemstem - supporting knowledge, innovation and technological advancement on the Steem Blockchain.
Contribute to Open Source with utopian.io
Learn how to contribute on our website and join the new open source economy.
Want to chat? Join the Utopian Community on Discord https://discord.gg/h52nFrV
Gracias por el apoyo. :)